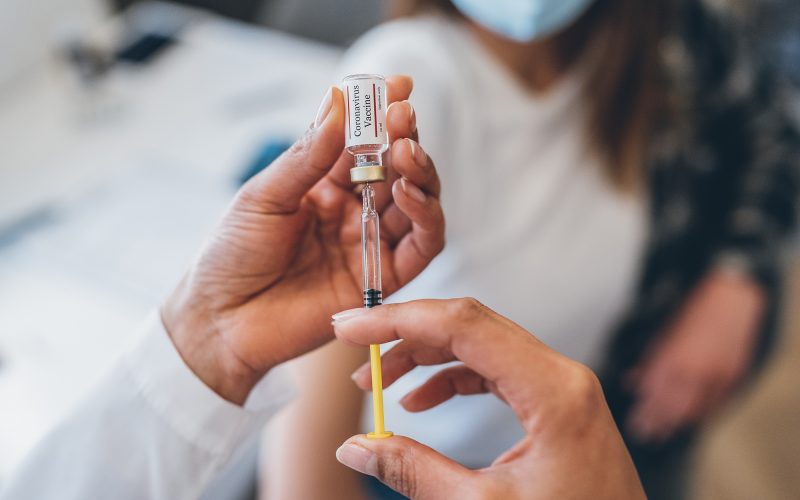
Da coronaepidemien gjorde sit indtog, talte man mere end nogensinde om vacciner. Epidemien og dens restriktioner betød, at mange følte, at deres liv var gået i stå, og de ventede med længsel efter en vaccine, der i et vist omfang kunne betyde, at de kunne vende tilbage til en hverdag, som man kendte den før epidemien.
Det havde indledningsvis lange udsigter. Vacciner er uhyre komplicerede at udvikle, og ingen havde turdet håbe på, at de kom så hurtigt, som de kom – og da slet ikke, at de viste sig så effektive. Det er uden sammenligning de hurtigste vacciner, der nogensinde er udviklet, og det har selvfølgelig rejst spørgsmålet, om de er udviklet for hurtigt. Er de nye vacciner overhovedet sikre?
Godkendelse af vacciner
Når der udvikles en vaccine eller enhver anden medicin, skal den gennem tre forskellige faser, hvor den testes på mennesker. Forud ligger selvfølgelig omfattende teoretiske og praktiske forsøg i både reagensglas og på dyr. Man tester så præparatet på en ganske lille gruppe forsøgspersoner. Hvis resultaterne her er gode, går man videre til fase 2, hvor flere forsøgspersoner deltager, inden man i 3. fase tester på flere tusinde personer. I denne fase får halvdelen af testpersonerne et placebo – typisk saltvand – så man kan sammenligne sygdomsudviklingen og bivirkninger mellem de to grupper. Normalt går der måneder eller endda år mellem hver fase, da alle resultater skal analyseres grundigt, og der skal indhentes ny tilladelse til fase 2-studier, hvis resultaterne ved fase 1 var lovende. I tilfældet med de nye coronavacciner var den ventetid skåret væk, da testfaserne blev sat i gang, allerede inden den fåregående var færdig. Man analyserede løbende på resultaterne, hvorfor man allerede d. 11. december 2020 kunne nødgodkende vaccinen fra Pfizer/BioNTech i USA. Ca. 10 dage senere kunne EU’s lægemiddelstyrelse, EMA, udstede en betinget godkendelse af samme præparat.
Godkendelse med forbehold?
For at kunne udstede en godkendelse af vacciner, skal der normalt foretages en analyse af vaccinens langtidsdata for virkning og bivirkninger. Det tager typisk 2-3 år, hvad der selvfølgelig ikke var tid til med covid-19-vaccinen. EMA’s betingede godkendelse blev givet, da fageksperter vurderede, at dokumentationen for effekt og sikkerhed var tilstrækkelig solid, så fordelene oversteg de teoretiske risici, som det indebar, når ikke alle langtidsdata endnu var tilgængelige. Når der udstedes en betinget godkendelse eller en nødgodkendelse, skal vaccineproducenten løbende forsyne myndighederne med yderligere data. Når alt data er indløbet og godkendt, kan den betingede godkendelse ændres til en normal godkendelse.
Hvem skal vaccineres mod COVID-19?
I skrivende stund tilbydes alle danskere over 12 år at blive vaccineret mod covid-19 med vaccine fra Pfizer/BioNtech eller Moderna. Invitationerne sker i en prioriteret rækkefølge, så de med størst risiko for alvorligt sygdomsforløb inviteres først. I praksis betyder det, at de ældste og særligt udsatte prioriteres først. Sidst prioriteres børn mellem 12-15 år. De har kun beskeden risiko for et alvorligt forløb.
Vaccination af børn
D. 17. juni meddelte Sundhedsstyrelsen på et pressemøde, at de anbefalede vaccinen til børn mellem 12-15 år for at styrke den samlede flokimmunitet. Den beslutning fandt børnelægernes formand Klaus Birkelund lidt forhastet:
”Jeg vil som børnelæge anbefale forældrene at afvente beslutningen, til vi har nogle flere informationer om den her vaccine”.
Klaus Birkelund Johansen, formand for børnelægerne, 17. juni 2021
Klaus Birkelund Johansens forbehold var bl.a. baseret på, at børn kun i meget sjældne tilfælde bliver alvorligt syge, når de bliver smittet med det nye coronavirus. Dermed afveg Sundhedsstyrelsens vaccinationsstrategi af børn mod covid-19 fra de generelle vaccinationsprincipper, hvor et bærende element er, at den, der bliver vaccineret, får en personlig sundhedsgevinst. Sundhedsstyrelsens primære argument for at vaccinere var, at vaccination af børn og unge ville beskytte andre befolkningsgrupper, hvorfor vaccination af dem var et middel og ikke et mål. Desuden savnede Klaus Birkelund Johansen data. De europæiske lægemyndigheder, EMA, gav d. 28. maj en godkendelse til Pfizer-BioNtechs vaccine til børn i alderen 12-15 år, men den godkendelse beror i nogles øjne på for få data. Det er i det lys, at Klaus Birkelund Johansen anbefalede, at man ventede med at vaccinere børn, indtil man vidste mere. På samme tidspunkt havde man i USA vaccineret 3 mio. børn, og børnelægerne ville gerne høre om deres erfaringer, før de anbefalede lignende tilgang i Danmark. I slutningen af juli var en del af den data tikket ind, og den gav anledning til en ny udmelding:
”Alvorlige bivirkninger har vist sig at være sjældne og ikke specielt alvorlige. Derfor er jeg mindre bekymret, end jeg har været. Vi fraråder ikke, at man skal tage imod vaccinen.”
Klaus Birkelund Johansen, formand for børnelægerne, 28. juli 2021